Khác biệt giữa bản sửa đổi của “Vericiguat”
←Trang mới: “{{Short description|Medication}} {{Infobox drug | drug_name = | INN = | type = <!-- empty --> | image = Vericiguat Structural formula V1.svg | width = | alt = | caption = <!-- Clinical data --> | pronounce = | tradename = Verquvo | Drugs.com = | MedlinePlus = | licence_EU = <!-- EMA uses INN (or special INN_EMA) --> | DailyMedID…” |
(Không có sự khác biệt)
|
Phiên bản lúc 03:37, ngày 7 tháng 8 năm 2021
Vericiguat, được bán dưới tên thương mại Verquvo, là một thuốc dùng để giảm nguy cơ tử vong do bệnh tim mạch và suy tim.[1][2] Thuốc được dùng qua đường uống.[1][2]
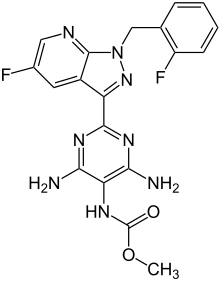 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Verquvo |
| Giấy phép |
|
| Dược đồ sử dụng | Đường uống |
| Nhóm thuốc | Chất hoạt hóa guanylate cyclase hoà tan |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý | |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| ECHA InfoCard | 100.247.370 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C19H16F2N8O2 |
| Khối lượng phân tử | 426,39 g·mol−1 |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
Tác dụng phụ thường thấy của thuốc bao gồm huyết áp thấp và giảm số lượng hồng cầu.[2]
Vericiguat là một chất kích thích guanylate cyclase hòa tan (sGC).[1] Thuốc được chấp thuận sử dụng y tế ở Hoa Kỳ vào tháng 1 năm 2021.[2][3]
Sử dụng trong y tế
Vericiguat được chỉ định để làm giảm nguy cơ tử vong do tim mạch và nhập viện do suy tim sau một đợt nhập viện điều trị suy tim hoặc cần dùng lợi tiểu đường tiêm tĩnh mạch ở người lớn mắc suy tim mạn tính có triệu chứng và phân suất tống máu nhỏ hơn 45%.[1][2]
Tác dụng phụ
Vericiguat gây hại cho thai nhi và không nên sử dụng ở phụ nữ mang thai.[2]
Lịch sử
Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chấp thuận vericiguat dựa trên bằng chứng từ một thử nghiệm lâm sàng (NCT02861534) bao gồm 5.050 bệnh nhân với độ tuổi từ 23 đến 98 có suy tim tiến triển xấu dần.[2] Thử nghiệm được thực hiện ở 694 địa điểm tại 42 quốc gia ở Châu Âu, Châu Á, Bắc và Nam Mỹ.[2] Thử nghiệm chọn những bệnh nhân có triệu chứng của suy tim tiến triển xấu dần.[2] Các bệnh nhân được nhận ngẫu nhiên vericiguat hoặc một viên giả dược 1 lần/ngày.[2] Cả bệnh nhân và nhân viên y tế đều không biết bệnh nhân sẽ nhận được vericiguat hay viên giả dược cho đến khi thử nghiệm kết thúc.[2]
Văn hóa và xã hội
Tình trạng pháp lý
Vào ngày 20 tháng 5 năm 2021, Ủy ban về các sản phẩm thuốc dùng cho người (CHMP) của Cơ quan Dược phẩm Châu Âu đã thông qua ý kiến tích cực, khuyến nghị cấp giấy phép lưu hành cho vericiguat, nhằm điều trị suy tim mạn tính có triệu chứng ở người lớn phân suất tống máu giảm.[4] Đơn vị đăng ký sản phẩm thuốc này là Bayer AG.
Tham khảo
- ^ a b c d e f “Verquvo- vericiguat tablet, film coated”. DailyMed. Truy cập ngày 9 tháng 2 năm 2021.
- ^ a b c d e f g h i j k l “Drug Trials Snapshot: Verquvo”. U.S. Food and Drug Administration (FDA). 8 tháng 2 năm 2021. Truy cập ngày 8 tháng 2 năm 2021. Bài viết này tích hợp văn bản từ nguồn này, vốn thuộc phạm vi công cộng.
- ^ “Verquvo: FDA-Approved Drugs”. U.S. Food and Drug Administration (FDA). Truy cập ngày 19 tháng 1 năm 2021.
- ^ “Verquvo: Pending EC decision”. European Medicines Agency. 20 tháng 5 năm 2021. Truy cập ngày 23 tháng 5 năm 2021. Text was copied from this source which is © European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
Đọc thêm
- Armstrong PW, Pieske B, Anstrom KJ, Ezekowitz J, Hernandez AF, Butler J, và đồng nghiệp (tháng 5 năm 2020). “Vericiguat in Patients with Heart Failure and Reduced Ejection Fraction”. N Engl J Med. 382 (20): 1883–1893. doi:10.1056/NEJMoa1915928. PMID 32222134.
Liên kết ngoài
- “Vericiguat”. Drug Information Portal. U.S. National Library of Medicine.
- Clinical trial number NCT02861534 for "A Study of Vericiguat in Participants With Heart Failure With Reduced Ejection Fraction (HFrEF) (MK-1242-001) (VICTORIA)" at ClinicalTrials.gov