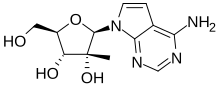
MK-608
MK-608 (7-deaza-2'-C-methyladenosine, 7DMA) là một loại thuốc chống vi-rút, một chất tương tự adenosine (một loại tương tự nucleoside). Ban đầu nó được Merck & Co. phát triển để điều trị viêm gan C, nhưng mặc dù kết quả đầy hứa hẹn trong nghiên cứu trên động vật,[1][2] cuối cùng đã không thành công trong các thử nghiệm lâm sàng.[3] Sau đó nó đã được sử dụng rộng rãi trong nghiên cứu virus và đã cho thấy hoạt động chống lại một loạt các virus, bao gồm sốt Dengue,[4] tick-borne vi rút viêm não,[5] poliovirus,[6][7] và gần đây nhất là vi rút Zika,[8][9] trong cả mô hình in vitro và động vật. Do đã thất bại trong các thử nghiệm lâm sàng ở người trước đây, nên MK-608 không có khả năng được phát triển dưới dạng thuốc kháng vi-rút, nhưng việc thiếu các lựa chọn điều trị cho các bệnh do virus mới nổi này có nghĩa là nhiều nghiên cứu tiếp tục sử dụng MK-608 và thuốc chống vi-rút liên quan thuốc.[10]
Xem thêm sửa
- BCX4430
- DZNep
- NITD008
Tham khảo sửa
- ^ Carroll SS, Ludmerer S, Handt L, Koeplinger K, Zhang NR, Graham D, Davies ME, MacCoss M, Hazuda D, Olsen DB. Robust antiviral efficacy upon administration of a nucleoside analog to hepatitis C virus-infected chimpanzees. Antimicrob Agents Chemother. 2009 Mar;53(3):926-34. doi:10.1128/AAC.01032-08.
- ^ Olsen DB, Davies ME, Handt L, Koeplinger K, Zhang NR, Ludmerer SW, Graham D, Liverton N, MacCoss M, Hazuda D, Carroll SS. Sustained viral response in a hepatitis C virus-infected chimpanzee via a combination of direct-acting antiviral agents. Antimicrob Agents Chemother. 2011 Feb;55(2):937-9. doi:10.1128/AAC.00990-10. PMID 21115793
- ^ Arnold JJ, Sharma SD, Feng JY, Ray AS, Smidansky ED, Kireeva ML, Cho A, Perry J, Vela JE, Park Y, Xu Y, Tian Y, Babusis D, Barauskus O, Peterson BR, Gnatt A, Kashlev M, Zhong W, Cameron CE. Sensitivity of mitochondrial transcription and resistance of RNA polymerase II dependent nuclear transcription to antiviral ribonucleosides. PLoS Pathog. 2012;8(11):e1003030. PMID 23166498 Toàn văn tại PMC: 3499576 doi:10.1371/journal.ppat.1003030
- ^ Schul W, Liu W, Xu HY, Flamand M, Vasudevan SG. A dengue fever viremia model in mice shows reduction in viral replication and suppression of the inflammatory response after treatment with antiviral drugs. J Infect Dis. 2007 Mar 1;195(5):665-74. PMID 17262707
- ^ Eyer L, Valdés JJ, Gil VA, Nencka R, Hřebabecký H, Šála M, Salát J, Černý J, Palus M, De Clercq E, Růžek D. Nucleoside inhibitors of tick-borne encephalitis virus. Antimicrob Agents Chemother. 2015 Sep;59(9):5483-93. doi:10.1128/AAC.00807-15. PMID 26124166
- ^ Goris N, De Palma A, Toussaint JF, Musch I, Neyts J, De Clercq K. 2'-C-methylcytidine as a potent and selective inhibitor of the replication of foot-and-mouth disease virus. Antiviral Res. 2007 Mar;73(3):161-8. PMID 17055073
- ^ Wu R, Smidansky ED, Oh HS, Takhampunya R, Padmanabhan R, Cameron CE, Peterson BR. Synthesis of a 6-methyl-7-deaza analogue of adenosine that potently inhibits replication of polio and dengue viruses. J Med Chem. 2010 Nov 25;53(22):7958-66. doi:10.1021/jm100593s. PMID 20964406 Toàn văn tại PMC: 2990348
- ^ Eyer L, Nencka R, Huvarová I, Palus M, Joao Alves M, Gould EA, De Clercq E, Růžek D. Nucleoside inhibitors of Zika virus. J Infect Dis. 2016 Sep 1;214(5):707-11. PMID 27234417 doi:10.1093/infdis/jiw226
- ^ Zmurko J, Marques RE, Schols D, Verbeken E, Kaptein SJ, Neyts J. The Viral Polymerase Inhibitor 7-Deaza-2'-C-Methyladenosine Is a Potent Inhibitor of In Vitro Zika Virus Replication and Delays Disease Progression in a Robust Mouse Infection Model. PLoS Negl Trop Dis. 2016 May 10;10(5):e0004695. doi:10.1371/journal.pntd.0004695. PMID 27163257
- ^ Vittori S, Dal Ben D, Lambertucci C, Marucci G, Volpini R, Cristalli G. Antiviral Properties of Deazaadenine Nucleoside Derivatives. Current Medicinal Chemistry December 2006, 13(29):3529-3552. doi:10.2174/092986706779026228