Tegaserod
Tegaserod là một chất chủ vận 5-HT4 do Novartis sản xuất và được bán dưới tên Zelnorm và Zelmac để kiểm soát hội chứng ruột kích thích và táo bón.[1] Được FDA chấp thuận vào năm 2002, sau đó nó đã bị loại khỏi thị trường vào năm 2007 do những lo ngại của FDA về các tác dụng phụ có hại cho tim mạch. Trước đó, đây là loại thuốc duy nhất được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ phê duyệt để giúp giảm đau bụng, đầy hơi và táo bón liên quan đến hội chứng ruột kích thích. Công dụng của nó cũng được chấp thuận để điều trị táo bón vô căn mãn tính.[2]
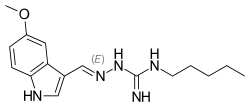 | |
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Zelnorm, Zelmac |
| AHFS/Drugs.com | Chuyên khảo |
| Danh mục cho thai kỳ | |
| Dược đồ sử dụng | Oral |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Sinh khả dụng | 10% |
| Liên kết protein huyết tương | 98% |
| Chuyển hóa dược phẩm | Gastric và Gan |
| Chu kỳ bán rã sinh học | 11 ± 5 hours |
| Bài tiết | Fecal and Thận |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEMBL | |
| ECHA InfoCard | 100.158.793 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C16H23N5O |
| Khối lượng phân tử | 301.39 g/mol |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Cơ chế hoạt động
sửaThuốc có chức năng như một chất kích thích vận động, đạt được hiệu quả điều trị mong muốn thông qua kích hoạt các thụ thể 5-HT4 của hệ thống thần kinh ruột trong đường tiêu hóa. Nó cũng kích thích nhu động đường tiêu hóa và phản xạ nhu động, và được cho là làm giảm đau bụng.[3] Ngoài ra, tegaserod là chất đối kháng thụ thể 5-HT2B.[4]
Rút khỏi thị trường
sửaVào ngày 30 tháng 3 năm 2007, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ đã yêu cầu Novartis rút Zelnorm khỏi giá.[5] FDA cáo buộc mối quan hệ giữa đơn thuốc và tăng nguy cơ đau tim hoặc đột quỵ. Một phân tích dữ liệu thu thập được trên 18.000 bệnh nhân đã chứng minh các biến cố tim mạch bất lợi ở 13 trong số 11.614 bệnh nhân được điều trị bằng Zelnorm (tỷ lệ 0,11%) so với 1 trong số 7.031 bệnh nhân được điều trị bằng giả dược (tỷ lệ 0,01%). Novartis cáo buộc tất cả các bệnh nhân bị ảnh hưởng đều mắc bệnh tim mạch từ trước hoặc các yếu tố nguy cơ như vậy, và cáo buộc thêm rằng không có mối quan hệ nhân quả nào giữa việc sử dụng tegaserod và các sự kiện tim mạch đã được chứng minh.[6] Cùng ngày với thông báo của FDA, Novartis Cosmetics Canada tuyên bố rằng họ đang tạm dừng tiếp thị và bán thuốc ở Canada để đáp ứng yêu cầu từ Bộ Y tế Canada.[7] Trong một nghiên cứu đoàn hệ lớn dựa trên cơ sở dữ liệu bảo hiểm y tế của Hoa Kỳ, không có sự gia tăng nào về nguy cơ biến cố tim mạch được tìm thấy khi điều trị bằng tegaserod.[8] Hiện tại, tegaserod chỉ có thể được sử dụng trong các tình huống khẩn cấp chỉ với sự cho phép trước của FDA.[9] [Cần cập nhật?]
Tham khảo
sửa- ^ “New Data for Zelnorm”. Bản gốc lưu trữ ngày 9 tháng 12 năm 2007. Truy cập ngày 30 tháng 3 năm 2007.
- ^ “FDA approves first treatment for women with irritable-bowel syndrome”. Bản gốc lưu trữ ngày 5 tháng 2 năm 2007. Truy cập ngày 30 tháng 3 năm 2007.
- ^ Rossi, S. (2004). Australian Medicines Handbook. Adelaide: Health Communication Network. ISBN 0-9578521-4-2.
- ^ Beattie DT, Smith JA, Marquess D, và đồng nghiệp (tháng 11 năm 2004). “The 5-HT4 receptor agonist, tegaserod, is a potent 5-HT2B receptor antagonist in vitro and in vivo”. Br. J. Pharmacol. 143 (5): 549–60. doi:10.1038/sj.bjp.0705929. PMC 1575425. PMID 15466450.
- ^ “FDA Announces Discontinued Marketing of GI Drug, Zelnorm, for Safety Reasons”. FDA Press Release. ngày 30 tháng 3 năm 2007.
- ^ “Zelnorm” (PDF). Novartis. Bản gốc (PDF) lưu trữ ngày 10 tháng 4 năm 2007. Truy cập ngày 30 tháng 3 năm 2007.
- ^ “Novartis suspends Canadian marketing and sales of Zelnorm in response to request from Health Canada”. Bản gốc lưu trữ ngày 5 tháng 6 năm 2007. Truy cập ngày 30 tháng 3 năm 2007.
- ^ Loughlin J, Quinn S, Rivero E, Wong J, Huang J, Kralstein J, Earnest DL, Seeger JD (2010). “Tegaserod and the Risk of Cardiovascular Ischemic Events: An Observational Cohort Study”. J Cardiovasc Pharmacol Ther. 15 (2): 151–7. doi:10.1177/1074248409360357. PMID 20200325.
- ^ http://www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsandProviders/ucm103223.htm