Bortezomib
Bortezomib (BAN, INN và USAN; được quảng cáo là Velcade của Takeda Oncology; chemobort của Cytogen và Bortecad của Cadila Healthcare) là một loại thuốc chống ung thư và là chất ức chế proteaome điều trị đầu tiên được sử dụng ở người. Proteasomes là phức hợp tế bào phá vỡ protein. Trong một số bệnh ung thư, các protein thường tiêu diệt tế bào ung thư bị phá vỡ quá nhanh. Bortezomib làm gián đoạn quá trình này và cho phép các protein đó tiêu diệt các tế bào ung thư. Nó được chấp thuận ở Mỹ và Châu Âu để điều trị tái phát nhiều u nguyên bào tủy và tế bào lympho.[1][2][3] Trong đa u tủy, các đáp ứng lâm sàng hoàn toàn đã đạt được ở những bệnh nhân mắc bệnh khó chữa hoặc tiến triển nhanh.
 | |
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Velcade by Takeda Oncology, Chemobort by Cytogen Pharma |
| Đồng nghĩa | PS-341 |
| AHFS/Drugs.com | Chuyên khảo |
| MedlinePlus | a607007 |
| Giấy phép |
|
| Danh mục cho thai kỳ | |
| Dược đồ sử dụng | Subcutaneous, IV |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Liên kết protein huyết tương | 83% |
| Chuyển hóa dược phẩm | Gan, CYP extensively involved |
| Chu kỳ bán rã sinh học | 9 to 15 hours |
| Các định danh | |
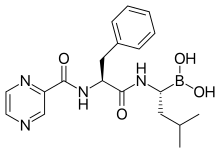
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| ChEMBL | |
| Phối tử ngân hàng dữ liệu protein | |
| ECHA InfoCard | 100.125.601 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C19H25BN4O4 |
| Khối lượng phân tử | 384.237 g/mol |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Nguồn gốc và sự phát triển sửa
Bortezomib ban đầu được tổng hợp vào năm 1995 tại Myogenics. Thuốc (PS-341) đã được thử nghiệm trong một thử nghiệm lâm sàng giai đoạn I nhỏ trên bệnh nhân đa u tủy. Nó đã được đưa đến các thử nghiệm lâm sàng tiếp theo bởi Millennium Pharmaceuticals vào tháng 10 năm 1999.
Vào tháng 5 năm 2003, bảy năm sau khi tổng hợp ban đầu, bortezomib (được bán bởi Velcade bởi Công ty Dược phẩm Thiên niên kỷ) đã được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chấp thuận để sử dụng cho bệnh đa u tủy, dựa trên kết quả từ SUMMIT Thử nghiệm giai đoạn II.[4] Bortezomib được FDA Hoa Kỳ chấp thuận điều trị ban đầu cho bệnh nhân đa u tủy xương vào năm 2008 [5]
Sau đó vào tháng 8 năm 2014, Cơ quan quản lý này đã phê duyệt Velcade cho việc rút lui bệnh nhân trưởng thành mắc bệnh đa u tủy [6] trước đó đã đáp ứng với liệu pháp Velcade và tái phát ít nhất sáu tháng sau khi hoàn thành điều trị trước đó.
Dược lý sửa
Kết cấu sửa
Thuốc là một dipeptide được bảo vệ N và có thể được viết là Pyz-Phe-boroLeu, viết tắt của axit pyrazinoic, phenylalanine và Leucine với axit boronic thay vì axit carboxylic.
Cơ chế sửa
Nguyên tử boron trong bortezomib liên kết vị trí xúc tác của proteaome 26S [7] với ái lực cao và tính đặc hiệu. Trong các tế bào bình thường, proteasome điều chỉnh sự biểu hiện và chức năng của protein bằng cách giáng hóa protein đã được ubiquitin hóa, đồng thời cũng giáng hóa cả các các protein bất thường hoặc bị cuộn gập sai. Dữ liệu lâm sàng và tiền lâm sàng hỗ trợ vai trò của proteasome trong việc duy trì kiểu hình bất tử của tế bào đa u tủy, và dữ liệu nuôi cấy tế bào và xenograft cho thấy proteasome có thể cũng có chức năng tương tự trong ung thư khối u rắn. Mặc dù nhiều cơ chế có khả năng liên quan, ức chế proteasome có thể ngăn chặn sự giáng hóa của các yếu tố pro-apoptotic (các yếu tố kích thích sự gây chết tế bào theo lập trình), do đó gây ra cái chết tế bào được lập trình trong các tế bào ung thư. Gần đây, người ta đã phát hiện ra rằng bortezomib gây ra sự thay đổi nhanh chóng và mạnh mẽ về mức độ của các peptide nội bào được sản xuất bởi proteasome.[8] Một số peptide nội bào đã được chứng minh là có hoạt tính sinh học, và do đó, tác dụng của bortezomib đối với mức độ của peptide nội bào có thể góp phần vào tác dụng sinh học và/hoặc tác dụng phụ của thuốc.
Dược động học và dược lực học sửa
Sau khi tiêm dưới da, nồng độ đỉnh trong huyết tương là ~ 25-50 nM và đỉnh này được duy trì trong 1-2 giờ. Sau khi tiêm tĩnh mạch, nồng độ đỉnh trong huyết tương là ~ 500 nM nhưng chỉ trong ~ 5 phút, sau đó nồng độ giảm nhanh khi thuốc phân phối đến các mô (thể tích phân phối là ~ 500 L).[9][10] Cả hai tuyến cung cấp phơi nhiễm thuốc bằng nhau và hiệu quả điều trị thường tương đương. Nửa đời thải trừ là 9 giờ15 và thuốc được loại bỏ chủ yếu bằng chuyển hóa ở gan.[11]
Dược lực học của bortezomib được xác định bằng cách định lượng ức chế proteasome trong các tế bào đơn nhân máu ngoại vi lấy từ bệnh nhân dùng thuốc.
Chi phí sửa
Ở Anh, NICE ban đầu đề nghị chống lại Velcade vào tháng 10 năm 2006 do chi phí khoảng 18.000 bảng mỗi bệnh nhân và vì các nghiên cứu được NICE xem xét cho biết họ chỉ có thể kéo dài tuổi thọ trung bình sáu tháng so với điều trị tiêu chuẩn.[12] Tuy nhiên, công ty sau đó đã đề xuất giảm chi phí liên kết hiệu suất cho đa u tủy,[13] và điều này đã được chấp nhận.[14]
Tác dụng phụ sửa
Tác dụng dạ dày-ruột (GI) và suy nhược là những tác dụng phụ phổ biến nhất.[15] Bortezomib có liên quan đến bệnh thần kinh ngoại biên ở 30% bệnh nhân dẫn đến đau. Điều này có thể tồi tệ hơn ở những bệnh nhân bị bệnh thần kinh từ trước. Ngoài ra, ức chế tủy gây giảm bạch cầu và giảm tiểu cầu cũng có thể xảy ra và bị giới hạn liều. Tuy nhiên, những tác dụng phụ này thường nhẹ so với ghép tủy xương và các lựa chọn điều trị khác cho bệnh nhân mắc bệnh tiến triển. Bortezomib có liên quan đến tỷ lệ bệnh zona cao,[16] mặc dù acyclovir dự phòng có thể làm giảm nguy cơ mắc bệnh này.[17]
Tác dụng phụ ở mắt như chalazion hoặc hordeolum (stye) có thể phổ biến hơn ở phụ nữ và đã dẫn đến ngừng điều trị.[18] Viêm thận kẽ cấp tính cũng đã được báo cáo.[19]
Tương tác thuốc sửa
Polyphenol có nguồn gốc từ chiết xuất trà xanh bao gồm epigallocatechin gallate (EGCG), được dự kiến sẽ có tác dụng hiệp đồng, thay vào đó đã được tìm thấy để làm giảm hiệu quả của bortezomib trong các thí nghiệm nuôi cấy tế bào.[20]
Hiệu quả điều trị sửa
Hai thử nghiệm nhãn mở, giai đoạn II (SUMMIT và CREST) đã xác định hiệu quả của bortezomib 1.3 mg/m 2 (có hoặc không có dexamethasone) được tiêm bằng bolus tiêm tĩnh mạch vào các ngày 1,4,8 và 11 của chu kỳ 21 ngày trong tối đa tám chu kỳ ở những bệnh nhân được điều trị trước nặng với đa u nguyên bào tái phát/tái phát.[21] Thử nghiệm APEX giai đoạn III đã chứng minh tính ưu việt của bortezomib 1.3 mg/m 2 trong chế độ điều trị bằng dexamethasone liều cao (ví dụ TTP trung bình 6,2 so với 3,5 tháng và tỷ lệ sống 1 năm 80% so với 66%).[21]
Sử dụng thử nghiệm sửa
Bortezomib đã được thử nghiệm cho bệnh lupus ban đỏ hệ thống (SLE) và dường như làm giảm hoạt động của bệnh và số lượng tế bào plasma, tuy nhiên 7 trong số 12 bệnh nhân đã bỏ thuốc do tác dụng phụ, một số trong đó là nghiêm trọng.[22] Bortezomib đã được nghiên cứu để điều trị thải ghép qua trung gian kháng thể của thận ghép. Một nghiên cứu cho thấy rằng việc sử dụng globulin miễn dịch tiêm tĩnh mạch liều cao kết hợp với chế độ điều trị dựa trên bortezomib dường như rất hữu ích, đặc biệt khi so sánh với một nhóm bệnh nhân được điều trị bằng globulin miễn dịch tiêm tĩnh mạch liều thấp, plasmapheresis và rituximab.[23]
Xem thêm sửa
- Ixazomib, một chất ức chế proteasome được đưa ra bằng miệng
Tham khảo sửa
- ^ Takimoto CH, Calvo E. "Principles of Oncologic Pharmacotherapy" Lưu trữ 2009-05-15 tại Wayback Machine in Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (Eds) Cancer Management: A Multidisciplinary Approach Lưu trữ 2013-10-04 tại Wayback Machine. 11 ed. 2008.
- ^ House, Douglas W. (ngày 9 tháng 10 năm 2014). “FDA clears Velcade label expansion”. Seeking Alpha.
- ^ Haberfeld, H biên tập (2016). Austria-Codex (bằng tiếng Đức). Vienna: Österreichischer Apothekerverlag.
- ^ Adams J, Kauffman M (2004). “Development of the Proteasome Inhibitor Velcade (Bortezomib)”. Cancer Invest. 22 (2): 304–11. doi:10.1081/CNV-120030218. PMID 15199612.
- ^ “Hoa Kỳ Department of Health and Human Services”. fda.gov. ngày 23 tháng 6 năm 2008.
- ^ “Millenium: The Takeda Oncology Company”. .millennium.com. ngày 8 tháng 8 năm 2014. Bản gốc lưu trữ ngày 1 tháng 11 năm 2018.
- ^ Bonvini P, Zorzi E, Basso G, Rosolen A (2007). “Bortezomib-mediated 26S proteasome inhibition causes cell-cycle arrest and induces apoptosis in CD-30+ anaplastic large cell lymphoma”. Leukemia. 21 (4): 838–42. doi:10.1038/sj.leu.2404528. PMID 17268529.
- ^ Gelman JS, Sironi J, Berezniuk I, Dasgupta S, Castro LM, Gozzo FC, Ferro ES, Fricker LD (2013). “Alterations of the intracellular peptidome in response to the proteasome inhibitor bortezomib”. PLOS ONE. 8 (1): e53263. doi:10.1371/journal.pone.0053263. PMC 3538785. PMID 23308178.
- ^ Reece DE, Sullivan D, Lonial S, Mohrbacher AF, Chatta G, Shustik C, Burris H 3rd, Venkatakrishnan K, Neuwirth R, Riordan WJ, Karol M, von Moltke LL, Acharya M, Zannikos P, Keith Stewart A (2011). “Pharmacokinetic and pharmacodynamic study of two doses of bortezomib in patients with relapsed multiple myeloma”. Cancer Chemother. Pharmacol. 67 (1): 57–67. doi:10.1007/s00280-010-1283-3. PMC 3951913. PMID 20306195.
- ^ Voorhees PM, Dees EC, O'Neil B, Orlowski RZ (2003). “The proteasome as a target for cancer therapy”. Clin Cancer Res. 9 (17): 6316–25. PMID 14695130.
- ^ Moreau P, Pylypenko H, Grosicki S, Karamanesht I, Leleu X, Grishunina M, Rekhtman G, Masliak Z, Robak T, Shubina A, Arnulf B, Kropff M, Cavet J, Esseltine DL, Feng H, Girgis S, van de Velde H, Deraedt W, Harousseau JL (2011). “Subcutaneous versus intravenous administration of bortezomib in patients with relapsed multiple myeloma: a randomised, phase 3, non-inferiority study”. The Lancet Oncology. 12 (5): 431–40. doi:10.1016/s1470-2045(11)70081-x. PMID 21507715.
- ^ “NHS watchdog rejects cancer drug”. BBC News UK. ngày 20 tháng 10 năm 2006. Truy cập ngày 14 tháng 8 năm 2009.
- ^ “Summary of VELCADE Response Scheme” (PDF). Bản gốc (PDF) lưu trữ ngày 19 tháng 4 năm 2009. Truy cập ngày 14 tháng 8 năm 2009.
- ^ “More Velcade-Style Risk-Sharing In The UK?”. Euro Pharma Today. ngày 21 tháng 1 năm 2009. Bản gốc lưu trữ ngày 10 tháng 7 năm 2011. Truy cập ngày 14 tháng 8 năm 2009.
- ^ “Highlights Of Prescribing Information” (PDF). Bản gốc (PDF) lưu trữ ngày 19 tháng 2 năm 2009. Truy cập ngày 17 tháng 8 năm 2019.
- ^ Oakervee HE, Popat R, Curry N, và đồng nghiệp (2005). “PAD combination therapy (PS-341/bortezomib, doxorubicin and dexamethasone) for previously untreated patients with multiple myeloma”. Br J Haematol. 129 (6): 755–62. doi:10.1111/j.1365-2141.2005.05519.x. PMID 15953001.
- ^ Pour L.; Adam Z.; Buresova L.; và đồng nghiệp (2009). “Varicella-zoster virus prophylaxis with low-dose acyclovir in patients with multiple myeloma treated with bortezomib”. Clinical Lymphoma & Myeloma. 9 (2): 151–3. doi:10.3816/CLM.2009.n.036. PMID 19406726.
- ^ Dennis, Michael; Maoz, Asaf; Hughes, David; Sanchorawala, Vaishali; Sloan, J. Mark; Sarosiek, Shayna (2019). “Bortezomib ocular toxicities: Outcomes with ketotifen”. American Journal of Hematology (bằng tiếng Anh). 0 (3): E80–E82. doi:10.1002/ajh.25382. ISSN 1096-8652. PMID 30575098.
- ^ Cheungpasitporn, Wisit; Leung, Nelson; Rajkumar, S. Vincent; Cornell, Lynn D.; Sethi, Sanjeev; Angioi, Andrea; Fervenza, Fernando C. (2015). “Bortezomib-induced acute interstitial nephritis”. Nephrol. Dial. Transplant. 30 (7): 1225–1229. doi:10.1093/ndt/gfv222. PMID 26109684.
- ^ Golden, EB; Lam, PY; Kardosh, A; Gaffney, KJ; Cadenas, E; Louie, SG; Petasis, NA; Chen, TC; Schönthal, AH (ngày 4 tháng 6 năm 2009). “Green tea polyphenols block the anticancer effects of bortezomib and other boronic acid-based proteasome inhibitors”. Blood. 113 (23): 5927–37. doi:10.1182/blood-2008-07-171389. PMID 19190249.
- ^ a b Curran M, McKeage K (2009). “Bortezomib: A Review of its Use in Patients with Multiple Myeloma”. Drugs. 69 (7): 859–888. doi:10.2165/00003495-200969070-00006. PMID 19441872. Bản gốc lưu trữ ngày 8 tháng 10 năm 2011. Truy cập ngày 26 tháng 3 năm 2010.
- ^ Alexanter T; và đồng nghiệp (2015). “The proteasome inhibitior bortezomib depletes plasma cells and ameliorates clinical manifestations of refractory systemic lupus erythematosus”. Ann Rheum Dis. 74 (7): 1474–8. doi:10.1136/annrheumdis-2014-206016. PMC 4484251. PMID 25710470.
- ^ Nils Lachmann, Michael Duerr, Constanze Schönemann, Axel Pruß, Klemens Budde, and Johannes Waiser, "Treatment of Antibody-Mediated Renal Allograft Rejection: Improving Step by Step," Journal of Immunology Research, vol. 2017, Article ID 6872046, 9 pages, 2017. https://doi.org/10.1155/2017/6872046.
Liên kết ngoài sửa
- [1]
- Bệnh nhân u tủy vận động để tiếp cận với một loại thuốc ung thư kéo dài cuộc sống
- Trang web Dược phẩm Thiên niên kỷ trên Velcade
- Nhiều bài viết của Tổ chức nghiên cứu Myeloma về Velcade
- Bài viết của Tổ chức Myeloma International trên Velcade Lưu trữ 2016-03-04 tại Wayback Machine
- Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ về Velcade
- Trang web dành riêng cho khán giả châu Âu