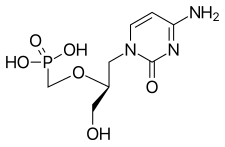
Cidofovir
Cidofovir (tên thương hiệu Vistide) là thuốc kháng vi-rút tiêm chủ yếu được sử dụng để điều trị viêm võng mạc do cytomegalovirus (CMV) (nhiễm trùng võng mạc mắt) ở người bị AIDS.[2][3]
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Vistide |
| AHFS/Drugs.com | Chuyên khảo |
| Giấy phép | |
| Danh mục cho thai kỳ | |
| Dược đồ sử dụng | IV |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý | |
| Dữ liệu dược động học | |
| Sinh khả dụng | complete |
| Liên kết protein huyết tương | <6% |
| Chu kỳ bán rã sinh học | 2.6 hours (active metabolites: 15-65 hours) |
| Bài tiết | renal The above pharmacokinetic parameters are measured for cidofovir used in conjunction with probenecid.[1] |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| ChEBI | |
| ChEMBL | |
| NIAID ChemDB | |
| ECHA InfoCard | 100.166.433 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C8H14N3O6P |
| Khối lượng phân tử | 279.187 g/mol |
| Mẫu 3D (Jmol) | |
| Sự quay riêng | -97.3 |
| Điểm nóng chảy | 260 °C (500 °F) |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Cidofovir đã được phê duyệt cho sử dụng y tế vào năm 1996.[4]
Sử dụng y tế
sửaVirus DNA
sửaDấu hiệu duy nhất của nó đã nhận được sự chấp thuận theo quy định trên toàn thế giới là viêm võng mạc do cytomegalovirus.[2][3] Cidofovir cũng đã cho thấy hiệu quả trong điều trị nhiễm HSV kháng aciclovir.[5] Cidofovir cũng đã được nghiên cứu như là một phương pháp điều trị bệnh não chất trắng đa ổ tiến triển với các báo cáo trường hợp thành công về việc sử dụng nó.[6] Mặc dù vậy, loại thuốc này không chứng minh được hiệu quả trong các nghiên cứu có kiểm soát.[7] Cidofovir có thể có hiệu quả chống bệnh đậu mùa và có thể được sử dụng trên cơ sở hạn chế trong trường hợp xảy ra sự cố sinh học liên quan đến các trường hợp bệnh đậu mùa.[8] Brincidofovir, một dẫn xuất cidofovir với hoạt tính cao hơn nhiều so với bệnh đậu mùa có thể dùng đường uống đã được phát triển.[9] Nó có tác dụng ức chế sự nhân lên của virus varicella-zoster trong ống nghiệm mặc dù cho đến nay chưa có thử nghiệm lâm sàng nào được thực hiện, có thể là do sự phong phú của các lựa chọn thay thế an toàn hơn như aciclovir.[10] Cidofovir cho thấy hoạt động chống vi rút BK trong một nhóm người nhận ghép.[11] Cidofovir đang bị điều tra như một liệu pháp bổ sung intralesional chống papillomatosis do HPV.[12][13]
Nó lần đầu tiên nhận được sự chấp thuận của FDA vào ngày 26 tháng 6 năm 1996,[14] phê duyệt TGA vào ngày 30 tháng 4 năm 1998 [3] và phê duyệt EMA vào ngày 23 tháng 4 năm 1997.[15]
Nó đã được sử dụng tại chỗ để điều trị mụn cóc.[16]
Khác
sửaNó đã được đề xuất như là một tác nhân chống độc, do sự ức chế FGF2.[17][18]
Cách dùng
sửaCidofovir chỉ có sẵn dưới dạng thuốc tiêm tĩnh mạch. Cidofovir sẽ được dùng cùng với probenecid làm giảm tác dụng phụ cho thận.[19] Probenecid làm giảm độc tính trên thận bằng cách ức chế vận chuyển anion hữu cơ của các tế bào biểu mô ống gần của thận.[20] Ngoài ra, hydrat hóa phải được dùng cho bệnh nhân dùng cidofovir. Nên dùng 1 lít nước muối bình thường kết hợp với mỗi liều cidofovir.[19]
Cơ chế hoạt động
sửaChất chuyển hóa hoạt động của nó, cidofovir diphosphate, ức chế sự nhân lên của virus bằng cách ức chế chọn lọc DNA polymerase của virus.[3] Nó cũng ức chế polymerase của người nhưng hành động này yếu hơn 8-600 lần so với hành động của nó đối với polymerase DNA của virus.[3] Nó cũng kết hợp chính nó vào DNA virus do đó ức chế tổng hợp DNA của virus trong quá trình sinh sản.[3]
Nó có hoạt động in vitro chống lại các virus sau:[21]
- Virus herpes ở người
- Adenovirus
- Poxvirus ở người (bao gồm cả virus đậu mùa)
- Virus u nhú ở người
Lịch sử
sửaCidofovir được phát hiện tại Viện Hóa học hữu cơ và hóa sinh, Prague, bởi Antonín Holý, và được phát triển bởi Gilead Science [22] và được bán với tên thương hiệu Vistide bởi Gilead ở Hoa Kỳ và bởi Pfizer ở nơi khác.
Tổng hợp
sửaCidofovir có thể được tổng hợp từ một dẫn xuất pyrimidone và một dẫn xuất được bảo vệ của glycidol.[23]
Xem thêm
sửa- Brincidofovir, một sản phẩm mới của cidofovir có thể uống
Tham khảo
sửa- ^ Cundy, Kenneth C. "Clinical Pharmacokinetics of the Antiviral Nucleotide Analogues Cidofovir and Adefovir." Clinical Pharmacokinetics 36.2 (1999): 127-43.
- ^ a b “Vistide (cidofovir) dosing, indications, interactions, adverse effects, and more”. Medscape Reference. WebMD. Truy cập ngày 4 tháng 2 năm 2014.
- ^ a b c d e f “Product Information VISTIDE®”. TGA eBusiness Services. Gilead Sciences Pty Ltd. ngày 3 tháng 9 năm 2013. Truy cập ngày 5 tháng 2 năm 2014.
- ^ Long, Sarah S.; Pickering, Larry K.; Prober, Charles G. (2012). Principles and Practice of Pediatric Infectious Disease (bằng tiếng Anh). Elsevier Health Sciences. tr. 1502. ISBN 978-1437727029.
- ^ Chilukuri, S; Rosen, T (tháng 4 năm 2003). “Management of acyclovir-resistant herpes simplex virus”. Dermatologic Clinics. 21 (2): 311–20. doi:10.1016/S0733-8635(02)00093-1. PMID 12757254.
- ^ Segarra-Newnham M, Vodolo KM (tháng 6 năm 2001). “Use of cidofovir in progressive multifocal leukoencephalopathy”. Ann Pharmacother. 35 (6): 741–4. doi:10.1345/aph.10338. PMID 11408993.[liên kết hỏng]
- ^ De Gascun, C. F.; Carr, M. J. (2013). “Human polyomavirus reactivation: Disease pathogenesis and treatment approaches”. Clinical and Developmental Immunology. 2013: 1–27. doi:10.1155/2013/373579. PMC 3659475. PMID 23737811.
- ^ De Clercq E (tháng 7 năm 2002). “Cidofovir in the treatment of poxvirus infections”. Antiviral Res. 55 (1): 1–13. doi:10.1016/S0166-3542(02)00008-6. PMID 12076747.
- ^ Bradbury, J (tháng 3 năm 2002). “Orally available cidofovir derivative active against smallpox”. Lancet. 359 (9311): 1041. doi:10.1016/S0140-6736(02)08115-1. PMID 11937193.
- ^ Magee, WC; Hostetler, KY; Evans, DH (tháng 8 năm 2005). “Mechanism of Inhibition of Vaccinia Virus DNA Polymerase by Cidofovir Diphosphate”. Antimicrobial Agents and Chemotherapy. 49 (8): 3153–3162. doi:10.1128/AAC.49.8.3153-3162.2005. PMC 1196213. PMID 16048917.
- ^ Araya CE, Lew JF, Fennell RS, Neiberger RE, Dharnidharka VR (tháng 2 năm 2006). “Intermediate-dose cidofovir without probenecid in the treatment of BK virus allograft nephropathy”. Pediatr Transplant. 10 (1): 32–7. doi:10.1111/j.1399-3046.2005.00391.x. PMID 16499584. Bản gốc lưu trữ ngày 5 tháng 1 năm 2013.
- ^ Broekema FI, Dikkers FG (tháng 8 năm 2008). “Side-effects of cidofovir in the treatment of recurrent respiratory papillomatosis”. Eur Arch Otorhinolaryngol. 265 (8): 871–9. doi:10.1007/s00405-008-0658-0. PMC 2441494. PMID 18458927.
- ^ Soma MA, Albert DM (tháng 2 năm 2008). “Cidofovir: to use or not to use?”. Curr Opin Otolaryngol Head Neck Surg. 16 (1): 86–90. doi:10.1097/MOO.0b013e3282f43408. PMID 18197029.
- ^ “Cidofovir Monograph for Professionals - Drugs.com”. Drugs.com. American Society of Health-System Pharmacists. Truy cập ngày 5 tháng 2 năm 2014.
- ^ “Vistide: EPAR -Product Information” (PDF). European Medicines Agency. Gilead Sciences International Ltd. ngày 7 tháng 11 năm 2013. Bản gốc (PDF) lưu trữ ngày 22 tháng 2 năm 2014. Truy cập ngày 5 tháng 2 năm 2014.
- ^ Fernández-Morano, T; del Boz J; González-Carrascosa M (2011). “Topical cidofovir for viral warts in children”. J Eur Acad Dermatol Venereol. 25 (12): 1487–9. doi:10.1111/j.1468-3083.2010.03961.x. PMID 21261749.
- ^ Liekens S, Gijsbers S, Vanstreels E, Daelemans D, De Clercq E, Hatse S (tháng 3 năm 2007). “The nucleotide analog cidofovir suppresses basic fibroblast growth factor (FGF2) expression and signaling and induces apoptosis in FGF2-overexpressing endothelial cells”. Mol. Pharmacol. 71 (3): 695–703. doi:10.1124/mol.106.026559. PMID 17158200.
- ^ Liekens S (2008). “Regulation of cancer progression by inhibition of angiogenesis and induction of apoptosis”. Verh. K. Acad. Geneeskd. Belg. 70 (3): 175–91. PMID 18669159.
- ^ a b “Details” (PDF). www.gilead.com. Truy cập ngày 5 tháng 6 năm 2019.
- ^ Lacy, S. "Effect of Oral Probenecid Coadministration on the Chronic Toxicity and Pharmacokinetics of Intravenous Cidofovir in Cynomolgus Monkeys.
- ^ Safrin, S; Cherrington, J; Jaffe, HS (tháng 9 năm 1997). “Clinical uses of cidofovir”. Reviews in Medical Virology. 7 (3): 145–156. doi:10.1002/(SICI)1099-1654(199709)7:3<145::AID-RMV196>3.0.CO;2-0. PMID 10398479.
- ^ “Press Releases: Gilead”. Bản gốc lưu trữ ngày 8 tháng 2 năm 2013. Truy cập ngày 5 tháng 12 năm 2007.
- ^ Brodfuehrer, P; Howell, Henry G.; Sapino, Chester; Vemishetti, Purushotham (1994). “A practical synthesis of (S)-HPMPC”. Tetrahedron Letters. 35 (20): 3243. doi:10.1016/S0040-4039(00)76875-4.