Iobenguane
Iobenguane, hay MIBG, là một chất tương tự aralkylguanidine của chất dẫn truyền thần kinh adrenergic norepinephrine và một dược phẩm phóng xạ. Nó hoạt động như một tác nhân ngăn chặn các tế bào thần kinh adrenergic. Khi được dán nhãn phóng xạ, nó có thể được sử dụng trong các kỹ thuật chẩn đoán y học hạt nhân cũng như trong các phương pháp điều trị chống ung thư thần kinh. Nó định vị vào mô adrenergic và do đó có thể được sử dụng để xác định vị trí của các khối u như pheochromocytomas và neuroblastomas. Với I-131, nó cũng có thể được sử dụng để loại bỏ các tế bào khối u chiếm và chuyển hóa norepinephrine.
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Đồng nghĩa | meta-iodobenzylguanidine mIBG, MIBG |
| Dược đồ sử dụng | Intravenous |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Các định danh | |
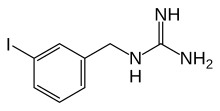
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| ChEMBL | |
| Dữ liệu hóa lý | |
| Công thức hóa học | C8H10IN3 |
| Khối lượng phân tử | 275.09 g/mol |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |

Nó định vị vào mô adrenergic và do đó có thể được sử dụng để xác định vị trí của các khối u [1] như pheochromocytomas và u nguyên bào thần kinh. Với I-131, nó cũng có thể được sử dụng để loại bỏ các tế bào khối u chiếm và chuyển hóa norepinephrine.
Cách sử dụng và cơ chế
sửaMIBG được hấp thụ và tích lũy trong các hạt của tế bào chromaffin tủy thượng thận, cũng như trong các hạt tế bào thần kinh adrenergic tiền synap. Quá trình xảy ra điều này có liên quan chặt chẽ với cơ chế được sử dụng bởi norepinephrine và công cụ vận chuyển in vivo. Chất vận chuyển norepinephrine (NET) có chức năng cung cấp sự hấp thu norepinephrine tại các đầu nối synap và tế bào chromaffin tuyến thượng thận. MIBG, bằng cách liên kết với NET, tìm thấy vai trò của nó trong hình ảnh và trị liệu.
Chuyển hóa và bài tiết
sửaDưới 10% liều dùng được chuyển hóa thành axit m-iodohippuric (MIHA), và cơ chế cho cách thức chuyển hóa này được sản xuất vẫn chưa được biết.
Thủ tục hình ảnh
sửaMIBG được dán nhãn bằng iod 131 hoặc 123 tập trung trong các khối u nội tiết, phổ biến nhất là u nguyên bào thần kinh, paragangliomas và pheochromocytomas. Nó cũng tích lũy trong các chất vận chuyển norepinephrine trong các dây thần kinh adrenergic trong tim, phổi, tủy thượng thận, tuyến nước bọt, gan và lá lách, cũng như trong các khối u bắt nguồn từ mào thần kinh. MIBG phục vụ như một sàng lọc xạ hình toàn thân, không xâm lấn cho các khối u tuyến, soma, lành tính và ác tính có nguồn gốc từ tuyến thượng thận. Nó có thể phát hiện cả bệnh nội và ngoại tiết. Các hình ảnh rất nhạy cảm và cụ thể. Iobenguane tập trung ở các thiết bị đầu cuối của tim và các cơ quan tự trị khác. Điều này cho phép sử dụng không xâm lấn như một đầu dò in vivo để nghiên cứu các hệ thống này. Một lượng lớn hợp chất đã được sử dụng trong các thử nghiệm để điều trị chọn lọc xạ trị đối với các tế bào pheochromocytomas ác tính cũng như u nguyên bào thần kinh.
Tác dụng phụ
sửaTác dụng phụ phổ biến sau khi chụp ảnh bao gồm giảm bạch cầu, giảm bạch cầu, thiếu máu, giảm tiểu cầu và mệt mỏi. Buồn nôn, nôn, tăng huyết áp và chóng mặt cũng đã được quan sát. 6,8% bệnh nhân trong một nghiên cứu đã nhận được liều điều trị của iobenguane đã phát triển bệnh bạch cầu cấp tính hoặc hội chứng myelodysplastic.
Phòng ngừa tuyến giáp
sửaỨc chế tuyến giáp với kali iodide (không hoạt động) được chỉ định cho xạ hình y học hạt nhân với iobenguane / mIBG. Điều này cạnh tranh ức chế sự hấp thu radioiodine, ngăn chặn mức độ phóng xạ quá mức trong tuyến giáp và giảm thiểu nguy cơ cắt bỏ tuyến giáp (trong trường hợp I-131). Nguy cơ tối thiểu của ung thư tuyến giáp cũng giảm do đó.
Liều lượng kali iodide được FDA phê chuẩn cho mục đích này như sau: trẻ sơ sinh dưới 1 tháng tuổi, 16 tuổi mg; trẻ 1 tháng đến 3 tuổi, 32 mg; trẻ em 3 tuổi đến 18 tuổi, 65 tuổi mg; người lớn 130 mg.[2] Tuy nhiên, một số nguồn khuyến nghị chế độ dùng thuốc thay thế.[3]
Không phải tất cả các nguồn đều đồng ý về thời gian cần thiết của phong tỏa tuyến giáp, mặc dù dường như đã đạt được thỏa thuận về sự cần thiết của phong tỏa đối với cả ứng dụng xạ trị và trị liệu của iobenguane. Iobenguane có bán trên thị trường được dán nhãn iod-123 và ghi nhãn sản phẩm khuyến nghị sử dụng kali iodide 1 giờ trước khi sử dụng dược phẩm phóng xạ cho tất cả các nhóm tuổi,[4] trong khi Hiệp hội Y học hạt nhân châu Âu khuyến nghị (đối với iobenguane được dán nhãn I- 131 hoặc I-123,) rằng việc sử dụng kali iodide bắt đầu một ngày trước khi dùng dược phẩm phóng xạ và tiếp tục cho đến ngày sau khi tiêm, ngoại trừ trẻ sơ sinh, không cần dùng liều kali iodide sau khi tiêm thuốc phóng xạ.[3]
Ghi nhãn sản phẩm để chẩn đoán iodine-131 iobenguane khuyến cáo sử dụng kali iodide một ngày trước khi tiêm và tiếp tục 5 đến 7 ngày sau đó.[5] Iodine-131 iobenguane được sử dụng cho mục đích điều trị đòi hỏi thời gian dùng thuốc khác nhau, bắt đầu 24-48 giờ trước khi tiêm iobenguane và tiếp tục 10-15 phút sau khi tiêm.[6]
Phương thức hình ảnh thay thế cho pheochromocytoma
sửaQuét PET / CT FDOPA đã được chứng minh là nhạy cảm gần như 100% để phát hiện pheochromocytomas, so với 90% đối với quét MIBG.[7][8][9] Tuy nhiên, các trung tâm cung cấp FDOPA PET / CT rất hiếm.
Các thử nghiệm lâm sàng
sửaIobenguane I 131 cho bệnh ung thư
sửaIobenguane I 131, được bán trên thị trường với tên thương mại Azedra, đã có một thử nghiệm lâm sàng như là một phương pháp điều trị cho pheochromocytoma ác tính, tái phát hoặc không thể phát hiện được, và FDA đã phê duyệt vào ngày 30 tháng 7 năm 2018. Thuốc được phát triển bởi Dược phẩm Progenics.[10][11]
Tham khảo
sửa- ^ Scarsbrook AF; Ganeshan A; Statham J; và đồng nghiệp (2007). “Anatomic and functional imaging of metastatic carcinoid tumors”. Radiographics. 27 (2): 455–77. doi:10.1148/rg.272065058. PMID 17374863.
- ^ Kowalsky RJ, Falen, SW. Radiopharmaceuticals in Nuclear Pharmacy and Nuclear Medicine. 2nd ed. Washington DC: American Pharmacists Association; 2004.
- ^ a b “Archived copy” (PDF). Bản gốc (PDF) lưu trữ ngày 7 tháng 10 năm 2011. Truy cập ngày 7 tháng 10 năm 2011.Quản lý CS1: bản lưu trữ là tiêu đề (liên kết)
- ^ “Bản sao đã lưu trữ” (PDF). Bản gốc (PDF) lưu trữ ngày 23 tháng 8 năm 2011. Truy cập ngày 17 tháng 8 năm 2019.
- ^ Iobenguane Sulfate I 131 Injection Diagnostic package insert. Bedford, MA: CIS-US, Inc. July 1999.
- ^ “Archived copy” (PDF). Bản gốc (PDF) lưu trữ ngày 7 tháng 10 năm 2011. Truy cập ngày 7 tháng 10 năm 2011.Quản lý CS1: bản lưu trữ là tiêu đề (liên kết)
- ^ 6-[18FFluorodopamine Positron Emission Tomographic (PET) Scanning for Diagnostic Localization of Pheochromocytoma. Pacek et al. 2001] full text
- ^ Pheochromocytoma Imaging Updated May 2017
- ^ Luster M, Karges W, Zeich K, Pauls S, Verburg FA, Dralle H, và đồng nghiệp (2010). “Clinical value of (18)F-fluorodihydroxyphenylalanine positron emission tomography/computed tomography ((18)F-DOPA PET/CT) for detecting pheochromocytoma”. European Journal of Nuclear Medicine and Molecular Imaging. 37 (3): 484–93. doi:10.1007/s00259-009-1294-7. PMID 19862519.
- ^ “AZEDRA® (iobenguane I 131) Jul 2018”. Bản gốc lưu trữ ngày 17 tháng 8 năm 2019. Truy cập ngày 17 tháng 8 năm 2019.
- ^ FDA approves first treatment for rare adrenal tumors Jul 2018