Gibbsit
Gibbsit, Al(OH)3, là một trong những dạng khoáng vật quan trọng của Nhôm hydroxide. Nó thường được đặt là γ-Al(OH)3 (nhưng đôi khi là α-Al(OH)3.[3]). Nó đôi khi còn được gọi là hydrargillite (hoặc hydrargyllite).
| Gibbsit | |
|---|---|
 Gibbsit từ Brasil | |
| Thông tin chung | |
| Thể loại | Khoáng vật hydroxide |
| Công thức hóa học | Al(OH)3 |
| Phân loại Strunz | 04.FE.10 |
| Phân loại Dana | 06.03.01.01 |
| Hệ tinh thể | Đơn nghiêng |
| Nhóm không gian | Hệ thoi 2/m lăng trụ |
| Ô đơn vị | a = 8.641 Å, b = 5.07 Å, c = 9.719 Å, Z = 8; |
| Nhận dạng | |
| Màu | Xanh nước biển, xanh lá, trắng xanh lá, xám, trắng xám |
| Dạng thường tinh thể | Dạng đất, dạng cầu, dạng thạch nhũ |
| Cát khai | Hoàn hảo ở mặt {001} |
| Vết vỡ | Khó vỡ |
| Độ cứng Mohs | 2.5 - 3 |
| Ánh | Ánh thủy tinh – ánh ngọc trai |
| Màu vết vạch | Trắng |
| Tính trong mờ | Trong mờ đến trong suốt |
| Mật độ | 2.3 đến 2.4. Trung bình là: 2.34 |
| Thuộc tính quang | Hai trục (+) |
| Khúc xạ kép | 0.0170-0.0180 |
| Góc 2V | 0 (theo lý thuyết); 0-5 (theo kết quả đo) |
| Huỳnh quang | Không phát quang |
| Tham chiếu | [1][2] |
Gibbsit là một quặng quan trọng của nhôm mà trong đó nó là một trong ba pha tạo nên đá bauxite. Bauxit thường được cho là một khoáng vật nhưng thực tế nó là một loại đá được tạo bởi khoáng vật hydroxide và oxyhydroxide như là gibbsite, boehmit (γ-AlO(OH)), và diaspore (α-AlO(OH)), cũng như là đất sét, bùn, oxit và hydroxide sắt.
Gibbsit có ba dạng đa hình: bayerit' (thường được đặt là α-Al(OH)3, nhưng đôi khi là β-Al(OH)3), doyleit, and nordstrandit. Gibbsit và bayerit ở hệ đơn nghiêng, trong khi doyleit và nordstrandit ở hệ ba nghiêng.
Cấu trúc
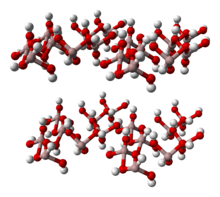
sửaCấu trúc của gibbsite khá thú vị và tương tự như cấu trúc cơ bản của mica. Các dạng cấu trúc cơ bản gắn các lớp bát diện nhôm hydroxide liên kết với nhau. Các bát diện được hợp thành từ ion nhôm với điện tích +3 liên kết với sáu đỉnh bát diện hydroxide với điện tích -1. Mỗi hydroxide liên kết với hai nguyên tử nhôm bởi vì một phần ba các bát diện thiếu mất một nguyên tử nhôm trung tâm. Kết quả tạo thành các lớp trung hòa về điện vì +3/6 = +1/2 (điện tích +3 của nhôm được chia cho sáu liên kết hydroxide giữa hai nguyên tử nhôm) và -1/2 = -1/2 (điện tích -1 của hydroxide chia đều cho hai nguyên tử nhôm); vì thế điện tích trung hòa. Các lớp gibbsit trung hòa về điện nên không có lực ion giữa các lớp. Các lớp chỉ được giữ bởi liên kết tàn dư yếu và kết quả khoáng vật có cát khai rất hoàn toàn.
Cấu trúc của Gibbsit có liên quan chặt chẽ với cấu trúc của brucit, Mg(OH)2. Tuy nhiên điện tích của magnesi (+2) trong brucit nhỏ hơn so với nhôm (+3) trong gibbsite không cần một phần ba các bát diện thiếu ion trung tâm để tạo thành các lớp trung hòa về điện. Sự đối xứng khác nhau giữa gibbsite và brucit là do cách mà các lớp dính với nhau khác nhau.
Cấu trúc lớp của gibbsit có thể gọi là "tiền than" cho khoáng vật corundum, Al2O3. Cấu trúc cơ bản của corundum tương tự như của gibbsite trừ việc thay thế hydroxide bằng nguyên tử oxy. Vì oxy có điện tích -2 nên các lớp không trung hòa về điện và chúng cần phải liên kết với các nguyên tử nhôm phía trên và phía dưới lớp đầu tiên tạo nên cấu trúc khung của corundum.
Gibbsit khá là thú vị bởi một lý do khác, đó là nó thường được tìm thấy như là một phần trong cấu trúc của khoáng vật khác. Các lớp nhôm hydroxide trung hòa được tìm thấy xen giữa các lớp silicat trong các nhóm khoáng vật sét quan trọng: illit, kaolinit và nhóm montmorillonit/smectit. Các lớp nhôm hydroxide đơn thường giống với cấu trúc đơn của gibbsite và được gọi là "lớp gibbsite".[4]
Etymology
sửaGibbsit được đặt tên theo nhà địa chất học George Gibbs (1776 – 1833), một nhà sưu tập khoáng vật người Mỹ.[5] Bộ sưu tập của G.Gibbs được lưu giữ bởi đại học Yale vào đầu thế kỉ 19.[6]
Xem thêm
sửa- Hurlbut, Cornelius S.; Klein, Cornelis, 1985, Manual of Mineralogy, 20th ed., ISBN 0-471-80580-7
- Webmineral Gibbsite
Tham chiếu
sửa- ^ http://www.webmineral.com/data/Gibbsite.shtml Webmineral
- ^ http://rruff.geo.arizona.edu/doclib/hom/gibbsite.pdf Handbook of Mineralogy
- ^ N.N. Greenwood and A. Earnshaw, "Chemistry of Elements", 2nd edition, Butterworth and Heinemann, 1997
- ^ GIBBSITE (Aluminum Hydroxide)
- ^ Gibbsite Mineral Data
- ^ Gibbsite: Gibbsite mineral information and data