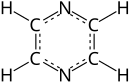
Pyrazine
Pyrazine là một hợp chất hữu cơ dị vòng thơm có công thức hóa học C4H4N2.
| Pyrazine | |||
|---|---|---|---|
| |||
| |||
| Danh pháp IUPAC | Pyrazine | ||
| Tên khác | 1,4-Diazabenzene, p-Diazine, 1,4-Diazine, Paradiazine, Piazine, UN 1325 | ||
| Nhận dạng | |||
| Số CAS | |||
| PubChem | |||
| Số EINECS | |||
| ChEBI | |||
| ChEMBL | |||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| Thuộc tính | |||
| Công thức phân tử | C4H4N2 | ||
| Khối lượng mol | 80.09 g/mol | ||
| Bề ngoài | White crystals | ||
| Khối lượng riêng | 1.031 g/cm³ | ||
| Điểm nóng chảy | 52 °C (325 K; 126 °F) | ||
| Điểm sôi | 115 °C (388 K; 239 °F) | ||
| Độ hòa tan trong nước | Soluble | ||
| Độ axit (pKa) | 0.37[1] (protonated pyrazine) | ||
| MagSus | -37.6·10−6 cm³/mol | ||
| Các nguy hiểm | |||
| NFPA 704 |
| ||
| Chỉ dẫn R | R11, R36/37/38 | ||
| Chỉ dẫn S | S16 , S26, S36 | ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
Pyrazine là một phân tử đối xứng với nhóm điểm D 2h. Pyrazine có tính base yếu hơn pyridine, pyridazine và pyrimidine.
Các dẫn xuất như phenazine nổi tiếng với các ứng dụng chống ung thư, kháng sinh và lợi tiểu.
Tetramethylpyrazine (còn được gọi là ligustrazine) được dùng để làm sạch anion superoxit và giảm sản xuất oxit nitric trong bạch cầu đa nhân của con người.[2]
Tổng hợp sửa
Nhiều phương pháp tồn tại để tổng hợp hữu cơ pyrazine và các dẫn xuất của nó. Một số trong số này là một trong những phản ứng tổng hợp lâu đời nhất vẫn được sử dụng.
Trong quá trình tổng hợp Strazeder Rugheimer pyrazine (1876), 2-chloroacetophenone được phản ứng với amonia thành amino ketone, sau đó cô đặc và sau đó được oxy hóa thành pyrazine.[3] Một biến thể là pyrazine tổng hợp Gutknecht (1879) cũng dựa trên này selfcondensation, nhưng khác nhau ở cách thức alpha-ketoamine được tổng hợp.[4][5]
Xem thêm sửa
- Benzen, một chất tương tự không có các nguyên tử nitơ
- Pyridazine, một chất tương tự với nguyên tử nitơ thứ hai ở vị trí 2
- Pyridine, một chất tương tự chỉ có một nguyên tử nitơ
- Pyrimidine, một chất tương tự với nguyên tử nitơ thứ hai ở vị trí 3
- Nhân hương phương cơ bản
Tham khảo sửa
- ^ Brown, H.C., et al., in Baude, E.A. and Nachod, F.C., Determination of Organic Structures by Physical Methods, Academic Press, New York, 1955.
- ^ Zhang, Zhaohui (2003). “Tetramethylpyrazine scavenges superoxide anion and decreases nitric oxide production in human polymorphonuclear leukocytes”. Life Sciences. 72 (22): 2465–2472. doi:10.1016/S0024-3205(03)00139-5.
- ^ Ueber die Einwirkung von Ammoniak auf Chloracetylbenzol (pp. 563–564) W. Staedel, L. Rügheimer doi:10.1002/cber.187600901174 Berichte der deutschen chemischen Gesellschaft Volume 9, Issue 1, pp. 563–564, 1876
- ^ Mittheilungen Ueber Nitrosoäthylmethylketon H. Gutknecht Berichte der deutschen chemischen Gesellschaft Volume 12, Issue 2, pp. 2290–2292, 1879 doi:10.1002/cber.187901202284
- ^ Heterocyclic chemistry T.L. Gilchrist ISBN 0-582-01421-2
- ^ G. Gastaldi, Gazz. Chim. Ital. 51, (1921) 233
- ^ Amines: Synthesis, Properties and Applications Stephen A. Lawrence 2004 Cambridge University Press ISBN 0-521-78284-8