Nickel tetracarbonyl
Nickel tetracarbonyl (các tên gọi khác: nickel carbonyl), là hợp chất cộng hóa trị của nickel, nó là bất thường đối với các hợp chất của kim loại này, ở nhiệt độ phòng nó là một chất lỏng không màu. Công thức hóa học của nó là Ni(CO)4. Nó là một chất cực độc trong ngành hóa học nickel[3] và có thể gây nguy hiểm cho tính mạng nếu uống nhầm hay qua đường da, do đó nó còn có tên gọi khác là "chất lỏng chết chóc". nickel tetracarbonyl cực kỳ dễ bay hơi. Nó bay hơi ngay ở nhiệt độ phòng. Hơi của nó có thể tự kích cháy ở nhiệt độ 60 °C (140 °F; 333 K). Hơi nickel carbonyl rất độc hại, hít là chết.
| Niken tetracacbonyl | |||
|---|---|---|---|
| |||
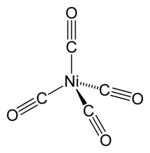 Cấu trúc 2D của niken tetracacbonyl | |||
| Danh pháp IUPAC | Tetracarbonylnickel | ||
| Tên khác | Niken tetracacbonyl Niken(0) tetracacbonyl | ||
| Nhận dạng | |||
| Số CAS | |||
| PubChem | |||
| Số EINECS | |||
| ChEBI | |||
| Số RTECS | QR6300000 | ||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| ChemSpider | |||
| Tham chiếu Beilstein | 6122797 | ||
| Tham chiếu Gmelin | 3135 | ||
| UNII | |||
| Thuộc tính | |||
| Công thức phân tử | Ni(CO)4 | ||
| Khối lượng mol | 171,0046 g/mol | ||
| Bề ngoài | chất lỏng không màu[1] | ||
| Mùi | mùi mốc,[1] như bụi gạch | ||
| Khối lượng riêng | 1,319 g/cm³ | ||
| Điểm nóng chảy | −17,2 °C (256,0 K; 1,0 °F) | ||
| Điểm sôi | 43 °C (316 K; 109 °F) | ||
| Độ hòa tan trong nước | 18 mg/100mL (10 °C)[cần dẫn nguồn] | ||
| Độ hòa tan | tan trong nhiều dung môi hữu cơ hòa tan trong axit nitric, nước cường toan | ||
| Áp suất hơi | 315 mmHg (20 °C)[1] | ||
| Độ nhớt | 3,05 x 10−4 Pa s | ||
| Cấu trúc | |||
| Tọa độ | Tứ phương | ||
| Hình dạng phân tử | Tứ phương | ||
| Mômen lưỡng cực | không | ||
| Nhiệt hóa học | |||
| Enthalpy hình thành ΔfH | −632 kJ/mol | ||
| DeltaHc | −1180 kJ/mol | ||
| Entropy mol tiêu chuẩn S | 320 J K−1 mol−1 | ||
| Các nguy hiểm | |||
| NFPA 704 |
| ||
| Giới hạn nổ | 2–34% | ||
| PEL | TWA 0,001 ppm (0,007 mg/m³)[1] | ||
| LC50 | 266 ppm (mèo, 30 phút) 35 ppm (thỏ, 30 phút) 94 ppm (chuột nhắt, 30 phút) 10 ppm (chuột nhắt, 10 phút)[2] | ||
| REL | TWA 0,001 ppm (0,007 mg/m³)[1] | ||
| IDLH | Ca [2 ppm][1] | ||
| Ký hiệu GHS |     | ||
| Chỉ dẫn nguy hiểm GHS | H225, H300, H310, H330, H351, H360D, H410 | ||
| Chỉ dẫn phòng ngừa GHS | P201, P202, P210, P233, P240, P241, P242, P243, P260, P271, P273, P280, P281, P284, P303+P361+P353, P304+P340, P308+P313, P310, P320, P370+P378, P391, P403+P233, P403+P235, P405, P501 | ||
| Các hợp chất liên quan | |||
| Nhóm chức liên quan | Sắt pentacacbonyl Đicoban octacacbonyl | ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
Giống như sắt pentacarbonyl, nickel tetracarbonyl là hợp chất có 18 cộng hóa trị.
Nickel kim loại ở nhiệt độ phòng có thể phản ứng với carbon monoxide (CO) để tạo ra nickel tetracarbonyl. Khi bị nung nóng nhẹ thì nickel tetracarbonyl bị phân hủy tạo ra carbon oxide và nickel kim loại. Hai phản ứng này tạo thành cơ sở cho quy trình Mond để sản xuất nickel tinh khiết.
Cấu trúc và liên kết
sửaTrong nickel tetracarbonyl, trạng thái oxy hóa của nickel được coi là bằng 0. Công thức là phù hợp với quy tắc 18 điện tử. Phân tử là tứ phương, với 4 phối tử carbonyl (carbon monoxide). Các nghiên cứu nhiễu xạ electron đã được thực hiện với phân tử này, và các khoảng cách Ni–C và C–O được tính toán tương ứng là 1,838(2) và 1,141(2) Å.[4]
Điều chế
sửaNi(CO)4 được Ludwig Mond tổng hợp lần đầu tiên năm 1890 bằng phản ứng trực tiếp của nickel kim loại với CO.[5] Công trình tiên phong này báo trước sự tồn tại của nhiều hợp chất carbonyl kim loại khác, bao gồm các hợp chất của vanadi, chromi, mangan, sắt và cobalt. Nó được sử dụng ở quy mô công nghiệp để tinh chế nickel vào cuối thế kỷ 19.[6]
Người ta cho carbon monoxide qua nickel không tinh khiết ở nhiệt độ từ 50 °C (323 K; 122 °F) trở lên. Tốc độ tối ưu diễn ra ở 130 °C.[7]
Phòng thí nghiệm
sửaNi(CO)4 không có sẵn ở quy mô thương mại. Nó được điều chế trong phòng thí nghiệm bằng carbonyl hóa bis(cyclooctadien)nickel(0) có sẵn ở quy mô thương mại.[8] Nó cũng có thể điều chế bằng phản ứng khử dung dịch amonia của nickel(II) sulfat với natri dithionit trong môi trường khí CO.[9]
Phản ứng
sửaKhử carbonyl nhiệt
sửaKhi nung nóng nhẹ thì Ni(CO)4 phân hủy thành carbon monoxide và nickel kim loại. Kết hợp với sự hình thành dễ dàng từ CO và ngay cả nickel không tinh khiết, sự phân hủy này là cơ sở cho quy trình Mond để tinh chế nickel. Sự phân hủy nhiệt diễn ra ở 180 °C và tăng lên theo nhiệt độ.[7]
Phản ứng với tác nhân ưa hạt nhân và tác nhân khử
sửaGiống như các carbonyl kim loại khác, Ni(CO)4 dễ bị tấn công bởi các tác nhân ưa hạt nhân. Sự tấn công có thể xảy ra ở nickel trung tâm dẫn tới sự thay thế phối tử CO, hoặc tại CO. Vì thế, các phối tử cho như triphenylphotphin phản ứng để tạo ra Ni(CO)3(PPh3) và Ni(CO)2(PPh3)2. Bipyridin và các phối tử có liên quan có phản ứng tương tự.[10] Sự thay thế đơn của nickel tetracarbonyl với các phối tử khác có thể sử dụng để xác định tham số electron Tolman, một phép đo khả năng cho hay rút electron của một phối tử nào đó.
Xử lý với các hydroxide tạo ra các cụm như [Ni5(CO)12]2− và [Ni6(CO)12]2−. Các hợp chất này cũng có thể thu được bằng cách khử nickel carbonyl.
Vì thế, xử lý Ni(CO)4 với các chất ưa hạt nhân carbon (Nu−) tạo ra các dẫn xuất acyl, như [Ni(CO)3C(O)Nu)]−.[11]
Phản ứng với tác nhân ưa điện tử và tác nhân oxy hóa
sửaNickel carbonyl cũng có thể bị oxy hóa. Clo oxy hóa nickel carbonyl thành NiCl2, giải phóng khí CO. Các halogen khác có phản ứng tương tự. Phản ứng này là phương pháp thuận tiện để tiêu hủy phần không mong muốn còn lại của hợp chất độc hại này.
Phản ứng của Ni(CO)4 với alkyl và aryl halide thường tạo ra các sản phẩm hữu cơ carbonyl hóa. Các halide vinyl, như PhCH=CHBr, được chuyển thành các este chưa bão hòa bằng xử lý với Ni(CO)4 và sau đó là bằng natri metoxide (CH3ONa). Các phản ứng như vậy cũng có thể tiến hành thông qua phản ứng cộng oxy hóa. Các haua allyl tạo ra các hợp chất π-allyl nickel, như (allyl)2Ni2Cl2:[12]
- 2Ni(CO)4 + 2ClCH2CH=CH2 → Ni2(μ-Cl)2(η3-C3H5)2 + 8CO↑
Độc tính
sửaBiểu hiện ngộ độc nickel tetracarbonyl được đặc trưng bởi hai giai đoạn của bệnh. Giai đoạn thứ nhất bao gồm đau đầu và tức ngực kéo dài vài giờ, thông thường được nối tiếp bằng sự thuyên giảm ngắn. Giai đoạn hai là viêm phổi do hóa chất, thông thường nó bắt đầu sau khoảng 16 giờ với các triệu chứng như ho, khó thở và cực kỳ mệt mỏi. Các triệu chứng này đạt đến độ nguy hiểm cao nhất sau khoảng 4 ngày, có thể gây tử vong do tổn thương tim mạch-hệ hô hấp hay suy thận cấp tính. Sự hồi phục thường là rất kéo dài, hay bị phức tạp hóa do sự kiệt sức, suy nhược và khó thở khi cố sức. Tổn thương vĩnh cửu hệ hô hấp là bất thường. Hiện vẫn còn tranh cãi về khả năng gây ung thư của nickel tetracarbonyl dạng khí. Tiêu chuẩn IDLH (NIOSH) là vào khoảng 2 ppm (14 mg/m³).
Liên kết ngoài
sửaTham khảo
sửa- ^ a b c d e f “NIOSH Pocket Guide to Chemical Hazards #0444”. Viện An toàn và Sức khỏe Nghề nghiệp Quốc gia Hoa Kỳ (NIOSH).
- ^ Lỗi chú thích: Thẻ
<ref>sai; không có nội dung trong thẻ ref có tênIDLH - ^ The Merck Index (ấn bản 7). Merck & Co.
- ^ Hedberg, L.; Iijima, T.; Hedberg, K. (1979). “Nickel tetracarbonyl, Ni(CO)4. I. Molecular Structure by Gaseous Electron Diffraction. II. Refinement of Quadratic Force Field”. The Journal of Chemical Physics. 70 (7): 3224–3229. doi:10.1063/1.437911.
- ^ Mond, L.; Langer, C.; Quincke, F. (1890). “Action of Carbon Monoxide on Nickel”. J. Chem. Soc. Trans. 57: 749–753. doi:10.1039/CT8905700749.
- ^ “The Extraction of Nickel from its Ores by the Mond Process”. Nature. 59 (1516): 63–64. 1898. doi:10.1038/059063a0.
- ^ a b Lascelles K.; Morgan L. G.; Nicholls D.; Beyersmann D. (2005), “Nickel Compounds”, Bách khoa toàn thư Ullmann về Hóa chất công nghiệp, Weinheim: Wiley-VCH, doi:10.1002/14356007.a17_235.pub2Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Jolly, P. W. (1982). “Nickel Tetracarbonyl”. Trong Abel, Edward W.; Stone, F. Gordon A.; Wilkinson, Geoffrey (biên tập). Comprehensive Organometallic Chemistry. I. Oxford: Pergamon Press. ISBN 0-08-025269-9.
- ^ F. Seel (1963). “Nickel Carbonyl”. Trong G. Brauer (biên tập). Handbook of Preparative Inorganic Chemistry, ấn bản lần 2. 2. NY: Academic Press. tr. 1747–1748.
- ^ Elschenbroich, C.; Salzer, A. (1992). Organometallics: A Concise Introduction (ấn bản 2). Weinheim: Wiley-VCH. ISBN 3-527-28165-7.
- ^ Pinhas, A. R. (2003). “Tetracarbonylnickel”. Encyclopedia of Reagents for Organic Synthesis, 8 Volume Set. Encyclopedia of Reagents for Organic Synthesis. John Wiley & Sons. doi:10.1002/047084289X.rt025m. ISBN 0471936235.
- ^ Semmelhack M. F.; Helquist P. M. (1972). “Reaction of Aryl Halides with π-Allylnickel Halides: Methallylbenzene”. Organic Syntheses. 52: 115.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết); Collective Volume, 6, tr. 722


