Ester
Bài viết này cần thêm chú thích nguồn gốc để kiểm chứng thông tin. |
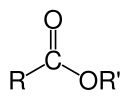
Trong hóa học, ester là một hợp chất hóa học được sinh ra từ một acid (hữu cơ hoặc vô cơ), trong đó, ít nhất một nhóm LIPOH (hydroxyl) được thay bằng nhóm alkyl (kiềm).[1] Thông thường, ester được cấu tạo từ acid carboxylic và alcohol. Glyceride, ester acid béo của glycerol, là loại ester rất quan trọng trong sinh học. Glyceride cũng là một loại lipid phổ biến và có mặt trong chất béo động vật và dầu thực vật. Ester có trọng lượng phân tử thấp và thường được sử dụng làm nước hoa. Ngoài ra, ester cũng được tìm thấy trong các loại tinh dầu và pheromone. Phosphoester tạo nên mạch khung của phân tử DNA. Các ester nitrat, chẳng hạn như nitroglycerin, là thành phần của thuốc nổ. Polyester lại là những chất dẻo quan trọng; trong polyester, các đơn phân được liên kết bởi các gốc ester. Ester thường có mùi thơm và được coi là dung môi tốt cho rất nhiều các chất dẻo, chất hóa dẻo, nhựa cây và sơn mài.[2] Đây cũng đồng thời là một trong chất bôi trơn tổng hợp lớn nhất trên thị trường.[3]
Tên gọi
sửaTên gốc hydrocarbon của alcohol (alkyl) + Tên gốc acid (ate) Ví dụ: CH3COOC2H5 đọc là ethyl acetate (hay ethyl ethanoate) Nếu rượu có tên riêng thì không cần biến đổi đuôi.
Phân loại
sửaCó bốn loại ester:
- Ester của acid đơn chức và alcohol đơn chức.
- Ester của acid đa chức và alcohol đơn chức. Loại này lại có thể chia thành các nhóm là ester trung hòa và ester acid.
- Ester của acid đơn chức và alcohol đa chức.
- Ester của acid đa chức và alcohol đa chức (ít gặp).
Tính chất vật lý
sửaEster của các loại rượu đơn chức và acid đơn chức (với số nguyên tử carbon không lớn lắm) thường là các chất lỏng, dễ bay hơi, có mùi thơm dễ chịu của các loại hoa quả khác nhau.
Nhiệt độ sôi của ester so với acid có cùng công thức phân tử thấp hơn rất nhiều vì không có sự tạo thành liên kết hydro. Tính tan của ester: tan ít trong nước.
Tính chất hoá học
sửaCác ester có một số tính chất chung như:
- Thủy phân trong môi trường acid (phản ứng thuận nghịch):
- RCOOR′ + H2O (H+) ↔ RCOOH + R′OH
- Thủy phân trong môi trường kiềm hay còn gọi là phản ứng xà phòng hóa.
- RCOOR’ + NaOH → RCOONa + R’OH
Một số tính chất riêng:
- Ester của acid formic: HCOOR có tính chất của một aldehyde.
- Ester của phenol bị thủy phân trong môi trường kiềm không tạo ra rượu. Ví dụ:
- CH3COOC6H5 + 2 NaOH → CH3COONa + C6H5ONa + H2O
- Ester của các rượu có liên kết pi khi thủy phân có thể tạo ra aldehyde hoặc keton. Ví dụ:
- CH3COOCH=CH2 + H2O → CH3COOH + CH3CHO
- Ester không no có phản ứng cộng và trùng hợp như hydrocarbon không no. Ví dụ phản ứng điều chế thủy tinh hữu cơ:
- nCH2=C(CH3)–COOCH3 →
(CH2=C(CH3)–COOCH3)(plexiglass)
- nCH2=C(CH3)–COOCH3 →
Đây là phản ứng trùng hợp với điều kiện về nhiệt độ, xúc tác thích hợp cùng áp suất cao.
Ester có thể bị khử bằng hydro:
RCOOR’ + H2 -> R’-H + R-H + CO/CO2/H2O (Mo-Ni/Co-Mo trên nền alumina, to,p)
Đây là bản chất của quá trình tái chế dầu ăn/mỡ động vật thành nhiên liệu.
Phương pháp điều chế
sửaCó thể điều chế ester bằng phản ứng giữa rượu đơn chức hoặc đa chức với acid hữu cơ đơn chức hoặc đa chức. Phản ứng này được gọi là phản ứng ester hóa. Ngoài ra còn có thể dùng acid tác dụng với alkyn hoặc cũng có thể cho phenol cộng với anhydrit acid.
Công thức tổng quát phản ứng ester hoá giữa rượu và acid carboxylic (Phản ứng thuận nghịch, điều kiện: H2SO4 đặc, to)
- R(COOH)x + xR'OH <=> R(COOR')x + xH2O
- yR(COOH)x + xR'(OH)y <=> Ry(COO)xyR'x + xyH2O
- xRCOOH + R'(OH)x <=> R'(OOCR)x + xH2O
Ví dụ:
- C2H5OH + CH3COOH <=> CH3COOC2H5 + H2O
Mùi của một số ester thông dụng
sửa- Isoamyl acetat có mùi chuối chín.
- Amyl format có mùi mận.
- Methyl salicylat có mùi dầu gió.
- Ethyl isovalerat có mùi táo.
- Ethyl butyrat và ethyl propionat có mùi dứa.
- Geranyl acetat có mùi hoa hồng.
- Methyl 2-aminobenzoat có mùi hoa cam.
- Benzyl acetat có mùi thơm hoa nhài.
Tham khảo
sửa- ^ IUPAC, Compendium of Chemical Terminology (Giản lược thuật ngữ hoá học), bản thứ 2 ("Gold Book") (1997). Bản đã chỉnh sửa trực tuyến: (2006–) "esters". doi:10.1351/goldbook.E02219
- ^ Cameron Wright (1986). A worker's guide to solvent hazards. The Group. tr. 48.
- ^ E. Richard Booser (ngày 21 tháng 12 năm 1993). CRC Handbook of Lubrication and Tribology, Volume III: Monitoring, Materials, Synthetic Lubricants, and Applications. CRC. tr. 237. ISBN 978-1-4200-5045-5.
[[1]]