Hydrocarbon
Bài viết này cần thêm chú thích nguồn gốc để kiểm chứng thông tin. |
Hydrocarbon là các hợp chất hữu cơ mà phân tử chỉ gồm carbon và hydro.[1] Chúng lại được chia thành hydrocarbon no, hydrocarbon không no, cycloalkan và hydrocarbon thơm.[2]
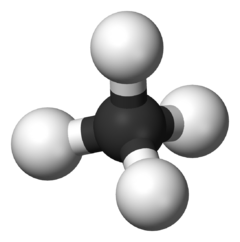
Hydrocarbon no
sửaHydrocarbon no là các Hydrocarbon mà các nguyên tử Carbon trong phân tử của nó liên kết với nhau bằng liên kết đơn. Còn những hóa trị còn lại được bão hòa bởi các nguyên tử hydrogen. Hydrocarbon no bao gồm hai loại: loại thứ nhất là alkan (hay còn gọi là paraffin) có công thức tổng quát là CnH2n+2 (n≥1) và loại thứ hai là cycloalkan với công thức tổng quát CnH2n (n≥3).
Alkan
sửa- Alkan là tên gọi theo danh pháp quốc tế các hợp chất hữu cơ.
- Paraffin là tên gọi xuất phát từ tiếng Latinh parum (nghĩa là "ít") và affinitas (nghĩa là "ái lực") vì chúng ít có khả năng phản ứng với các chất khác.
Các đồng đẳng của methane có công thức tổng quát CH4(CH2)n; ví dụ C2H6 (ethane), C3H8 (propane), C4H10 (butane),...
Tính chất vật lý
sửaỞ điều kiện thường
sửa-Từ 1C đến 4C: thể khí
-Từ 5C-17C: thể lỏng;
-Từ 18C trở lên: thể rắn.
- Nhiệt độ nóng chảy và nhiệt độ sôi tăng dần theo chiều tăng của phân tử khối (tức càng nhiều C sẽ có nhiệt độ sôi và nóng chảy càng cao).
- Khi số nguyên tử carbon tăng thì phân tử khối tăng nên nhiệt độ sôi tăng. Mạch carbon càng phân nhánh thì bề mặt tiếp xúc càng giảm nên lực hút giữa các phân tử giảm nên nhiệt đội sôi càng giảm do làm gia tăng cấu trúc cầu.
- Vì không có liên kết hydrogen với nước nên tất cả Hydrocarbon no đều không tan trong nước nhưng tan nhiều trong dung môi hữu cơ.
Tính chất hóa học
sửa- Phản ứng cháy: CH4 + 2O2 → CO2 + 2H2O
Tổng quát: CnH2n+2 + (3n+1)/2 O2 → n CO2 + (n+1)H2O
- Phản ứng thế halogen:
- CH4 + Cl2 → CH3Cl + HCl
- CH3Cl + Cl2 → CH2Cl2 + HCl
- CH2Cl2 + Cl2 → CHCl3 + HCl
- CHCl3 + Cl2 → CCl4 + HCl
- Phản ứng nhiệt phân: tùy theo điều kiện mà cho sản phẩm khác nhau
- Ngoài các tính chất trên, các hợp chất thuộc dãy đồng đẳng alkane còn có phản ứng cracking
Phương pháp điều chế
sửa- CnH2n +H2 (Pt, Ni hoặc Pd),nhiệt độ---> CnH2n+2
Ví dụ: C2H4 + H2 ---> C2H6
Hydrocarbon không no
sửaHydrocarbon không no là các Hydrocarbon có các liên kết bội (liên kết đôi hoặc liên kết ba) giữa các nguyên tử carbon. Tùy thuộc vào loại liên kết bội mà các Hydrocarbon không no được chia thành các loại sau:
- Alken: chứa 1 liên kết đôi
- Alkadien: chứa 2 liên kết đôi
- Alkyn: chứa 1 liên kết ba
Một số chất hydrocarbon không no
sửaTính chất vật lý
sửa- Chất khí từ 1 → 4C: khí không màu, không mùi.
- Chất lỏng từ 5 → 17C
- Từ 18C trở lên: chất rắn.
Tính chất hóa học
sửaỞ điều kiện bình thường, các hydrocarbon ánh sáng và nhiệt độ phản ứng thế với halogen. Phản ứng thế tuân theo quy tắc Markovnikov, theo đó hydro bậc cao hơn sẽ dễ bị thế hơn.
- Phản ứng oxy hóa hoàn toàn:
- CnH2n + O2 ==>n CO2 + n H2O
- CnH2n-2 + O2 ==>n CO2 + (n-1) H2O
phản ứng trên còn được gọi là phản ứng cháy (oxy hóa hoàn toàn);
- Phản ứng oxy hóa không hoàn toàn:
- CnH2n+2 ==>CnH2n + H2
Phản ứng trên còn được gọi là phản ứng tách hydro hay phản ứng dehydro hóa.
Phương pháp điều chế
sửaa) Khai thác từ dầu mỏ (khí đồng hành), khí tự nhiên qua các phương pháp cracking và chưng cất phân đoạn.
b) Phương pháp tăng mạch Carbon
C2H5OH ---> C2H4 + H2O
C2H6 ---> C2H4 +H2
C2H2 -(nhị hợp)--> C4H4
C2H2-(tam hợp)-->C6H6 (điều kiện)
C4H4 -(+ Hydrogen)---> C4H8
Cycloparaffin
sửaCycloparaffin là các hydrocarbon mà phân tử của nó gồm mạch các nguyên tử carbon khép kín thành vòng.
Cycloparaffin còn được gọi là polymethylene với công thức chung là CnH2n.
Hydrocarbon thơm
sửaHydrocarbon thơm là các hydrocarbon mà phân tử của chúng có các nhân benzen - C6H6. Một số hydrocarbon thơm khác có cấu trúc phức tạp hơn với một số nhân benzen được ngưng tụ như naphthalene-C10H8, anthracene-C14H10
Một số chất thuộc nhóm Hydrocarbon thơm
sửaTham khảo
sửa- ^ Silberberg, Martin (2004). Chemistry: The Molecular Nature Of Matter and Change. New York: McGraw-Hill Companies. ISBN 0-07-310169-9.
- ^ Schmidt, Roland; Griesbaum, Karl; Behr, Arno; Biedenkapp, Dieter; Voges, Heinz-Werner; Garbe, Dorothea; Paetz, Christian; Collin, Gerd; Mayer, Dieter; Höke, Hartmut (2014). “Hydrocarbons”. Ullmann's Encyclopedia of Industrial Chemistry. tr. 1–74. doi:10.1002/14356007.a13_227.pub3. ISBN 978-3-527-30673-2.
Liên kết ngoài
sửa- Hydrocarbon tại Từ điển bách khoa Việt Nam
- Hydrocarbon tại Encyclopædia Britannica (tiếng Anh)