Cation amoni bậc bốn
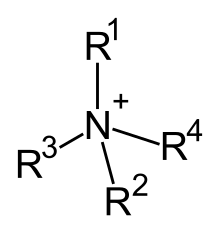
Các cation amoni bậc bốn, là các ion đa phân tử tích điện dương có cấu trúc NR+
4, R là một nhóm alkyl hoặc một nhóm aryl.[1] Không giống như ion ammoni (NH+
4) và các cation bậc ba, bậc hai hay bậc một, các cation bậc bốn tích điện vĩnh viễn, không phụ thuộc vào pH trong dung dịch của chúng. Các muối amoni bậc bốn hay các hợp chất amoni bậc bốn (gọi là các amin bậc bốn trong cách nói mỏ dầu) là các muối của các cation amoni bậc bốn.


Tổng hợp sửa
Các hợp chất amoni bậc bốn được điều chế bởi alkylation của bậc ba amin với halocarbon.[2] Trong các tài liệu cũ, điều này thường được gọi là phản ứng Menshutkin, tuy nhiên các nhà hóa học hiện đại thường gọi nó đơn giản là Bậc bốn hóa'.[3] Phản ứng có thể được sử dụng để tạo ra một hợp chất có độ dài chuỗi alkyl không đồng đều; ví dụ: khi tạo chất hoạt động bề mặt cation một trong những nhóm alkyl trên amin thường dài hơn các nhóm khác.[4] Một tổng hợp điển hình là cho benzalkonium chloride từ một alkyldimethylamine chuỗi dài và benzyl chloride:
- CH3(CH2)nN(CH3)2 + ClCH2C6H5 → [CH3(CH2)nN(CH3)2CH2C6H5]+Cl−
Phản ứng sửa
Các cation amoni bậc bốn không hợp lý đối với cả điện di, chất oxy hóa và axit. Chúng cũng ổn định đối với hầu hết nucleophile. Loại thứ hai được biểu thị bằng tính ổn định của các muối hydroxide như tetramethylammonium hydroxide và tetrabutylammonium hydroxide. Vì khả năng phục hồi của chúng, nhiều anion bất thường đã được phân lập thành muối amoni bậc bốn. Các ví dụ bao gồm tetramethylammonium pentafluoroxenate, có chứa ion pentafluoroxenate (XeF−
5) phản ứng cao. Permanganate có thể tan trong các dung môi hữu cơ, khi được triển khai như muối NBu+
4 của nó.[5][6]
Với các base đặc biệt mạnh mẽ, cation bậc bốn hạ bậc. Chúng trải qua quá trình sắp xếp lại Sommelet-Hauser[7] và sắp xếp lại Stevens,[8] cũng như dealkyl hóa trong điều kiện khắc nghiệt. Các cation amoni bậc bốn có chứa các đơn vị N-C-C-C-H cũng có thể trải qua loại bỏ Hofmann và hạ cấp Emde.
Ứng dụng sửa
Muối amoni bậc bốn được sử dụng như chất khử trùng, chất hoạt động bề mặt, chất làm mềm vải và như chất chống tĩnh điện (ví dụ như trong dầu gội). Trong chất lỏng chất làm mềm vải, muối chloride thường được sử dụng. Trong máy sấy chống bẩn, các muối sulfat thường được sử dụng. Gel diệt tinh trùng cũng chứa muối amoni bậc bốn.
Tham khảo sửa
- ^ International Union of Pure and Applied Chemistry. "quaternary ammonium compounds". Toàn văn bản Giản Lược Thuật Ngữ Hoá Học.
- ^ W. R. Brasen, C. R. Hauser (1954). “o-Methylethylbenzyl Alcohol”. Org. Synth. 34: 58. doi:10.15227/orgsyn.034.0058.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Smith, Michael B.; March, Jerry (2001), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (ấn bản 5), New York, NY: Wiley-Interscience, ISBN 0-471-58589-0
- ^ Kosswig, K. (2005), “Surfactants”, Bách khoa toàn thư Ullmann về Hóa chất công nghiệp, Weinheim: Wiley-VCH, doi:10.1002/14356007.a25_747
- ^ Herriott, Arthur W. (1977). “Purple benzene: Solubilization of anions in organic solvents”. J. Chem. Educ. 54 (4): 229. Bibcode:1977JChEd..54Q.229H. doi:10.1021/ed054p229.1.
- ^ Doheny, Anthony J., Jr.; Ganem, Bruce (1980). “Purple benzene revisited”. J. Chem. Educ. 57 (4): 308. Bibcode:1980JChEd..57..308D. doi:10.1021/ed057p308.1.
- ^ Brasen, W. R.; Hauser, C. R. (1963). “2-Methylbenzyldimethylamine”. Organic Syntheses.; Collective Volume, 4, tr. 585
- ^ Pine, Stanley H. (2011). “The Base-Promoted Rearrangements of Quaternary Ammonium Salts”. Organic Reactions. doi:10.1002/0471264180.or018.04. ISBN 0471264180.
- ^ Maximilian Lackner, Josef Peter Guggenbichler "Antimicrobial Surfaces" Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2013. doi:10.1002/14356007.q03_q01