Thali(I) carbonat
Hợp chất vô cơ
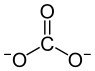
Thali(I) carbonat là một hợp chất vô cơ có công thức hóa học Tl2CO3. Nó là một muối carbonat màu trắng, có thể hòa tan trong nước. Nó không có hoặc rất ít ứng dụng thương mại. Nó được sản xuất bằng cách cho thali(III) hydroxide tác dụng với CO2[3].
| Thali(I) carbonat | |
|---|---|
 | |
| Danh pháp IUPAC | Thallium carbonate |
| Tên khác | Dithali monocarbonate Thalơ carbonat |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Số EINECS | |
| Số RTECS | XG4000000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| ChemSpider | |
| Thuộc tính | |
| Công thức phân tử | Tl2CO3 |
| Khối lượng mol | 468,7752 g/mol |
| Bề ngoài | tinh thể trắng |
| Mùi | không mùi |
| Khối lượng riêng | 7,11 g/cm³, rắn |
| Điểm nóng chảy | 272 °C (545 K; 522 °F) |
| Điểm sôi | |
| Độ hòa tan trong nước | 5,2 g/100 mL (25 °C) 27,2 g/100 mL (100 °C) |
| Độ hòa tan | không hòa tan trong alcohol, ether, aceton tạo phức với thioure |
| MagSus | −101.6·10−6 cm³/mol |
| Cấu trúc | |
| Cấu trúc tinh thể | hệ tinh thể đơn nghiêng |
| Các nguy hiểm | |
| Nguy hiểm chính | độc tính cao |
| NFPA 704 |
|
| LD50 | 21 mg/kg (chuột, miệng)[1] |
| Ký hiệu GHS |    [2] [2] |
| Báo hiệu GHS | Danger |
| Chỉ dẫn nguy hiểm GHS | H300, H330, H373, H411 |
| Chỉ dẫn phòng ngừa GHS | P260, P264, P270, P271, P273, P284, P301+P310, P304+P340, P310, P314, P320, P330, P391, P403+P233, P405, P501 |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
An toàn
sửaGiống như các hợp chất khác của thali, nó cực kỳ độc, với liều gây chết trung bình ở miệng là 21 mg/kg ở chuột. Do tính độc hại của nó, nó được liệt kê trong danh sách các chất cực kỳ nguy hiểm của Hoa Kỳ tính đến năm 2007[4].
Hợp chất khác
sửaTl2CO3 còn tạo một số hợp chất với CS(NH2)2, như Tl2CO3·8CS(NH2)2 là tinh thể màu vàng nhạt, nóng chảy ở 183–186 °C (361–367 °F; 456–459 K).[5]
Tham khảo
sửa- ^ “CDC - Immediately Dangerous to Life or Health Concentrations (IDLH): Thallium (soluble compounds, as Tl) - NIOSH Publications and Products”. www.cdc.gov (bằng tiếng Anh). 2 tháng 11 năm 2018. Lưu trữ bản gốc ngày 21 tháng 1 năm 2022. Truy cập ngày 26 tháng 2 năm 2022.
- ^ PubChem. “Thallium carbonate”. pubchem.ncbi.nlm.nih.gov (bằng tiếng Anh). Lưu trữ bản gốc ngày 12 tháng 12 năm 2021. Truy cập ngày 26 tháng 2 năm 2022.
- ^ Micke, Heinrich; Wolf, Hans Uwe (2005), “Thallium and Thallium Compounds”, Bách khoa toàn thư Ullmann về Hóa chất công nghiệp, Weinheim: Wiley-VCH, doi:10.1002/14356007.a26_607
- ^ “Emergency First Aid Treatment Guide THALLOUS CARBONATE”. Chemical Emergency Preparedness and Prevention. U.S. Environmental Protection Agency. Lưu trữ bản gốc ngày 5 tháng 3 năm 2014. Truy cập ngày 2 tháng 6 năm 2012.
- ^ Journal of inorganic and general chemistry (bằng tiếng Đức). 347. Johann Ambrosius Barth. 1966. tr. 160–166.
