Rubidi nitrat
Rubidi nitrat là một hợp chất vô cơ có thành phần gồm nguyên tố rubidi và nhóm nitrat, có công thức hóa học là RbNO3. Muối nitơ kim loại kiềm này có màu trắng và hòa tan trong nước.
| Rubidi nitrat | |
|---|---|
 | |
 | |
| Danh pháp IUPAC | Rubidium nitrate |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Số EINECS | |
| Số RTECS | QV0900000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| Thuộc tính | |
| Công thức phân tử | RbNO3 |
| Khối lượng mol | 147.473 g/mol |
| Bề ngoài | Chất rắn trắng hút ẩm |
| Khối lượng riêng | 3.11 g/cm³ |
| Điểm nóng chảy | 310 °C (583 K; 590 °F) phân hủy |
| Điểm sôi | 578 °C (851 K; 1.072 °F) |
| Độ hòa tan trong nước | 44.28 g/100 mL (16 °C), 65 g/100 mL (25 C)[1] |
| MagSus | −41.0·10−6 cm³/mol |
| Chiết suất (nD) | 1.524 |
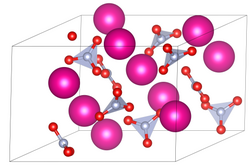
| Cấu trúc | |
| Cấu trúc tinh thể | trigonal |
| Nhóm không gian | P31 |
| Hằng số mạng | a = 10.474 Å, c = 7.443 Å [2] |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Tính chất
sửaRubidi nitrat tồn tại dưới dạng thức là một tinh thể màu trắng dạng bột hòa tan trong nước và ít tan trong axeton. Trong một bài kiểm tra thí nghiệm về việc bị đốt cháy dưới ngọn lửa, RbNO3 cháy phát ra ánh sáng màu tím hơi mờ.
Sử dụng
sửaCác hợp chất Rubidi có rất ít ứng dụng.[1] Giống như caesi nitrat, nó được sử dụng trong bức xạ hồng ngoại dùng tạo thành thành phần của pháo hoa, đóng vai trò là một chất màu và chất oxy hóa, ví dụ: trong các loại pháo và pháo sáng. Nó cũng được sử dụng làm nguyên liệu thô để điều chế các hợp chất rubidi khác và kim loại rubidi và sản xuất các chất xúc tác. Tuy có ứng dụng như trên, nhưng hợp chất này hiếm khi được sử dụng trong pháo hoa nhằm mục đích tạo ra pháo hoa màu đỏ tím.
Sản xuất
sửaRbNO3 có thể được điều chế bằng cách hòa tan kim loại rubidi, hoặc các hợp chất của rubidi của nó là hydroxide hoặc cacbonat trong axit nitric:
RbOH + HNO3 → RbNO3 + H2O
2 Rb + 2 HNO3 → 2 RbNO3 + H2
Tham khảo
sửa- ^ a b W. Lenk, H. Prinz, A. Steinmetz,"Rubidium and Rubidium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2010 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim. doi:10.1002/14356007.a23_473.pub2
- ^ Jutta Pohl, Dieter Pohl, Gunadi Adiwidjaja (1992). “Phase Transition in Rubidium Nitrate at 346 K and Structure at 296, 372, 413 and 437 K”. Acta Crystallographica Section B. B48: 160–166. doi:10.1107/S0108768191013459.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)